Bài tập trắc nghiệm Hóa Học 12 Bài 28: Luyện tập Tính chất của kim loại kiềm, kim loại kiềm thổ và hợp chất của chúng.
Câu hỏi trắc nghiệm (24 câu):
-
Câu 1:
Cho dãy các kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy tác dụng với H2O tạo dung dịch bazơ là:
- A.2.
- B.4.
- C.3.
- D.1.
-
Câu 2:
Dung dịch nào dưới đây dùng để phân biệt dung dịch KCl với dung dịch K2SO4?
- A.HCl
- B.NaOH
- C.H2SO4.
- D.BaCl2.
-
Câu 3:
Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước?
- A.Na
- B.Ba
- C.Ca
- D.Cu
-
Câu 4:
Cho các chất: (1) NaCl; (2) Na2CO3; (3) BaCl2; (4) Ca(OH)2; (5) Na3PO4; (6) Na2SO4. Những chất có thể làm mềm nước cứng tạm thời là:
- A.(1), (2), (3).
- B.(2); (4).
- C.(2); (4); (6).
- D.(2); (4); (5).
-
Câu 5:
Phát biểu nào sau đây không đúng?
- A.Trong dãy kim loại kiềm, đi từ Li đến Cs nhiệt độ nóng chảy giảm dần.
- B.Có thể dùng dung dịch Na2CO3 để làm mềm tất cả các loại nước cứng.
- C.Nhiệt độ nóng chảy và nhiệt độ sôi của kim loại kiềm thổ thấp hơn kim loại kiềm.
- D.Một trong những tác dụng của criolit trong quá trình sản xuất nhôm là làm tăng tính dẫn điện.
-
Câu 6:
Để phân biệt dung dịch CaCl2 với dung dịch NaCl, người ta dùng dung dịch:
- A.KNO3
- B.Na2CO3
- C.NaNO3
- D.HNO3
-
Câu 7:
Chất phản ứng được với CaCl2 là:
- A.HCl.
- B.Na2CO3.
- C.Mg(NO3)2.
- D.NaNO3.
-
Câu 8:
Cho các phản ứng xảy ra theo sơ đồ sau:
X1 + H2O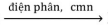 X2 + X3 + H2↑
X2 + X3 + H2↑
X2 + X4 → BaCO3↓ + K2CO3 + H2O
Chất X1, X4 lần lượt là:- A.KHCO3; Ba(OH)2.
- B.NaHCO3; Ba(OH)2.
- C.NaCl; Ba(HCO3)2.
- D.KCl; Ba(HCO3)2.
-
Câu 9:
Cho dãy kim loại: Na, Ba, Al, K, Mg. Số kim loại trong dãy phản ứng với lượng dư dung dịch FeCl3 có tạo kết tủa là:
- A.4.
- B.2.
- C.3.
- D.5.
-
Câu 10:
Kim loại nào sau đây khi cho vào dung dịch CuSO4 bị hòa tan hết và phản ứng tạo thành kết tủa gồm 2 chất:
- A.Na
- B.Fe
- C.Ba
- D.Zn
-
Câu 11:
Cho 26 gam hỗn hợp chất rắn A gồm Ca, MgO, Na2O tác dụng hết với dung dịch HCl 1M (vừa đủ) thu được dung dịch A trong đó có 23,4 gam NaCl. Giá trị của V là:
- A.0,09.
- B.1,02.
- C.0,72.
- D.1,08.
-
Câu 12:
Hấp thu hoàn toàn 4,48 lít khí CO2 (ở đkc) vào 500ml dung dịch hỗn hợp gồm NaOH 0,1M và Ba(OH)2 0,25M, sinh ra m gam kết tủa. Giá trị m là
- A.19,70.
- B.17,73.
- C.9,85.
- D.11,82.
-
Câu 13:
Cho một mẫu hợp kim Na-Ca-K tác dụng với nước (dư), thu được dung dịch X và 7,84 lít H2 (ở đktc). Thể tích dung dịch axit H2SO4 1,4M cần dùng để trung hoà dung dịch X là:
- A.125ml
- B.175ml
- C.500ml
- D.250ml
-
Câu 14:
Hòa tan hoàn toàn hỗn hợp gồm một kim loại hóa trị 1 và oxit kim loại hóa trị 2 vào nước dư. Sau khi phản ứng xong được 500 ml dd X chỉ chứa một chất tan duy nhất và 4,48 lít khí H2 (đktc). Nồng độ mol/l của dung dịch X là:
- A.0,3M
- B.0,25M
- C.0,2M
- D.0,4M
-
Câu 15:
Hấp thụ hoàn toàn 3,36 lít khí CO2 (điều kiện tiêu chuẩn) vào dung dịch chứa 0,15 mol NaOH và 0,1 mol Ba(OH)2 thu được m gam kết tủa. Giá trị của m là:
- A.14,775
- B.9,850
- C.29,550
- D.19,700
-
Câu 16:
Cho 7,1 gam hỗn hợp gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng với lượng dư dung dịch HCl loãng thu được 5,6 lít khí. Hai kim loại X, Y có thể là:
- A.K và Ba
- B.K và Ca.
- C.Na và Mg.
- D.Li và Be.
-
Câu 17:
Hòa tan hoàn toàn 8,94 gam hỗn hợp gồm Na, K và Ba vào nước thu được dung dịch X và 2,688 lit khí H2 (đktc) . Dung dịch Y gồm HCl và H2SO4 có tỉ lệ mol tương ứng: 4 : 1. Trung hòa dung dịch X bởi dung dịch Y, tổng khối lượng các muối được tạo ra là
- A.13,7
- B.12,78
- C.18,46
- D.14,62
-
Câu 18:
Cho các cặp dung dịch phản ứng với nhau:
(1) Na2CO3 + H2SO4
(2) NaHCO3 + FeCl3
(3) Na2CO3 + CaCl2
(4) NaHCO3 + Ba(OH)2
(5) (NH4)2SO4 + Ba(OH)2
(6) Na2S + AlCl3
Các cặp phản ứng có cả kết tủa và khí bay ra là
- A.5, 6
- B.2, 3, 5
- C.1, 3, 6
- D.2, 4, 6
-
Câu 19:
Hòa tan hỗn hợp Na2CO3, KHCO3, Ba(HCO3)2 (trong đó số mol Na2CO3 và KHCO3 bằng nhau) vào nước lọc thu được dung dịch X và m gam kết tủa Y. Biết X tác dụng vừa đủ 0,16mol NaOH hoặc 0,24mol HCl thì hết khí bay ra. Giá trị m là:
- A.7,88 g
- B.4,925 g
- C.1,97 g
- D.3,94g
-
Câu 20:
Tính khử của các nguyên tử Na, K, Al, Mg được xếp theo thứ tự tăng dần là:
- A.K, Na, Mg, Al
- B.Al, Mg, Na, K
- C.Mg, Al, Na, K
- D.Al, Mg, K, Na
-
Câu 21:
Chỉ dùng duy nhất một hóa chất nào dưới đây có thể phân biệt được 4 lọ mất nhãn chứa các dung dịch: AlCl3; ZnCl2; FeCl2 và NaCl.
- A.Dung dịch NaOH.
- B.Dung dịch Na2CO3
- C.Dung dịch AgNO3
- D.Nước amoniac
-
Câu 22:
Hấp thụ hoàn toàn 1,568 lít CO2 (đktc) vào 500ml dung dịch NaOH 0,16M thu được dung dịch X. Thêm 250 ml dung dich Y gồm BaCl2 0,16M và Ba(OH)2 a mol/l vào dung dịch X thu được 3,94 gam kết tủa và dung dịch Z. Tính a?
- A.0,02M
- B.0,04M
- C.0,03M
- D.0,015M
-
Câu 23:
Cho 2,22 gam hỗn hợp kim loại gồm K, Na và Ba vào nước được 500ml dung dịch X có pH = 13. Cô cạn dung dịch X được m gam chất rắn. m là:
- A.4,02
- B.3,42
- C.3,07
- D.3,05
-
Câu 24:
Hoà tan 46 gam một hỗn hợp Ba và hai kim loại kiềm A, B thuộc hai chu kì kế tiếp nhau vào nước thu được dung dịch C và 11,2 lít khí (đktc). Nếu thêm 0,18 mol Na2SO4 vào dung dịch C thì dung dịch sau phản ứng vẫn chưa kết tủa hết Ba. Nếu thêm 0,21 mol Na2SO4 vào dung dịch C thì dung dịch sau phản ứng còn dư Na2SO4. A và B là:
- A.Li và Na.
- B.Na và K.
- C.K và Rb.
- D.Rb và Cs.






Thảo luận về Bài viết